《周易》有云:“变则通,通则久。”在先进疗法日新月异的浪潮中,惟创新者进,惟笃行者强。宜明生物始终以开放拥抱变革,以实干笃定创新。
刚刚过去的2026年一季度,宜明生物依托在ATMP CRDMO行业的全领域、全链条技术平台与国际化布局及合规体系,与国内外多家行业领先企业达成重磅战略合作,在溶瘤病毒、基因治疗、免疫细胞治疗、干细胞治疗/再生医学等前沿赛道多点突破、全面开花。纷传的捷报,是过往深耕的积淀,更是后续高质量发展的坚实基点。
接下来与大家一同回顾宜明生物在第一季度中的精彩历程。
政府赋能:政企协同,共筑产业新高地
“天时、地利、人和”,宜明生物的蓬勃发展,既得益于时代机遇,更离不开各级政府的前瞻布局与精准护航。
2026年2月,北京市科委、中关村管委会出台《支持创新药合同研发生产机构提质增效的若干措施》,为CXO行业释放重磅政策红利。昌平“生命谷”凭借强大产业集聚效应,以政策引导、平台支撑、资本赋能构建全链条服务体系,在研发支持、人才引进、审评审批、空间保障等方面持续优化营商环境,形成一流产业生态。在政策加持与政府全方位支持下,宜明生物乘势而上,全面提速,北京基地也如期顺利建成投用。
在昌平区政府及相关部门支持下,宜明生物作为CGT产业重点企业,深度融入北京“医药健康产业三年行动计划”与医药健康产业“北部创新策源地”核心承载区建设。凭借ATMP CRDMO领军企业地位,公司积极承接多项国家、市级科技专项,并依托昌平“两区”建设政策优势,持续提升北京GMP基地国际化能力,以核心技术与产业能力反哺区域发展。

宜明生物北京基地GMP生产基地
政企协同聚力,正共同将“生命谷”打造为具有全球影响力的CGT创新高地,也为宜明生物从“国内领先”迈向“全球标杆”筑牢坚实后盾。
溶瘤病毒平台获国际认可
溶瘤病毒疗法历经百年发展,近年凭借技术迭代强势翻红。随着全球多款产品冲刺上市,市场热度持续攀升,同时对工艺开发与规模化量产提出更高要求。宜明生物依托自身新一代溶瘤病毒技术平台,深耕溶瘤病毒赛道,并在济南基地建设了专属生产线,为规模化量产提供坚实产能保障。

宜明生物济南GMP生产基地
一季度,公司在该领域接连收获重要成果。
助力美国长期合作伙伴ViroMissle自主研发的IDOV-Immune注射液成功获批FDA IND,宜明生物为此提供了工艺开发、GMP生产、方法学开发、检测放行、注册申报等全流程的CDMO服务。这是宜明生物助力获批的首个溶瘤病毒疗法临床试验许可,标志着公司在溶瘤病毒平台的生产体系已获得国际监管机构认可,具备支撑相关产品全球开发与上市的核心能力。
同时,宜明生物与多家中外知名药企围绕溶瘤病毒项目达成重磅战略合作,包括业内资深知名企业复诺健生物。宜明生物将为VG161以及VG201等核心项目提供中后期临床及商业化生产服务,其中VG161临床数据突出,曾登顶《自然》期刊。
众所周知,中后期临床试验及商业化生产是药品生产最严格的考验,要求产品批次一致性、稳定性与规模化能力均达到药监审评及长期市场供应标准,是“每一次都必须完美交付”的极致追求。客户将核心管线托付,是对公司技术能力、质量体系、供应链可靠性与长期保障能力的高度信任。
此次合作也标志着宜明生物病毒生产平台实现从“研发生产”到“支撑上市”的关键跨越,成为合作伙伴产品上市与市场布局的重要产能支柱与战略保障。
基因治疗领域深化合作
在AAV基因治疗领域,宜明生物与长期战略合作伙伴因诺惟康持续深化合作,再度携手为其新一代眼科基因治疗候选药物提供全流程CDMO服务。双方已有多个合作项目获批中美两地IND,还曾共同创造“9个月冲刺获批FDA IND”的行业奇迹。
严苛监管下的持续获批,见证了经得起全球考验的合规体系;多次可靠与高效的交付,业已沉淀为可复制、可规模化的产业化路径。截至目前,宜明生物已支持数十个AAV基因治疗项目获批IND,更有多个项目推进至临床三期阶段,覆盖20余种疾病领域,必将以全链条CRDMO能力全面助力基因治疗产业高质量发展。
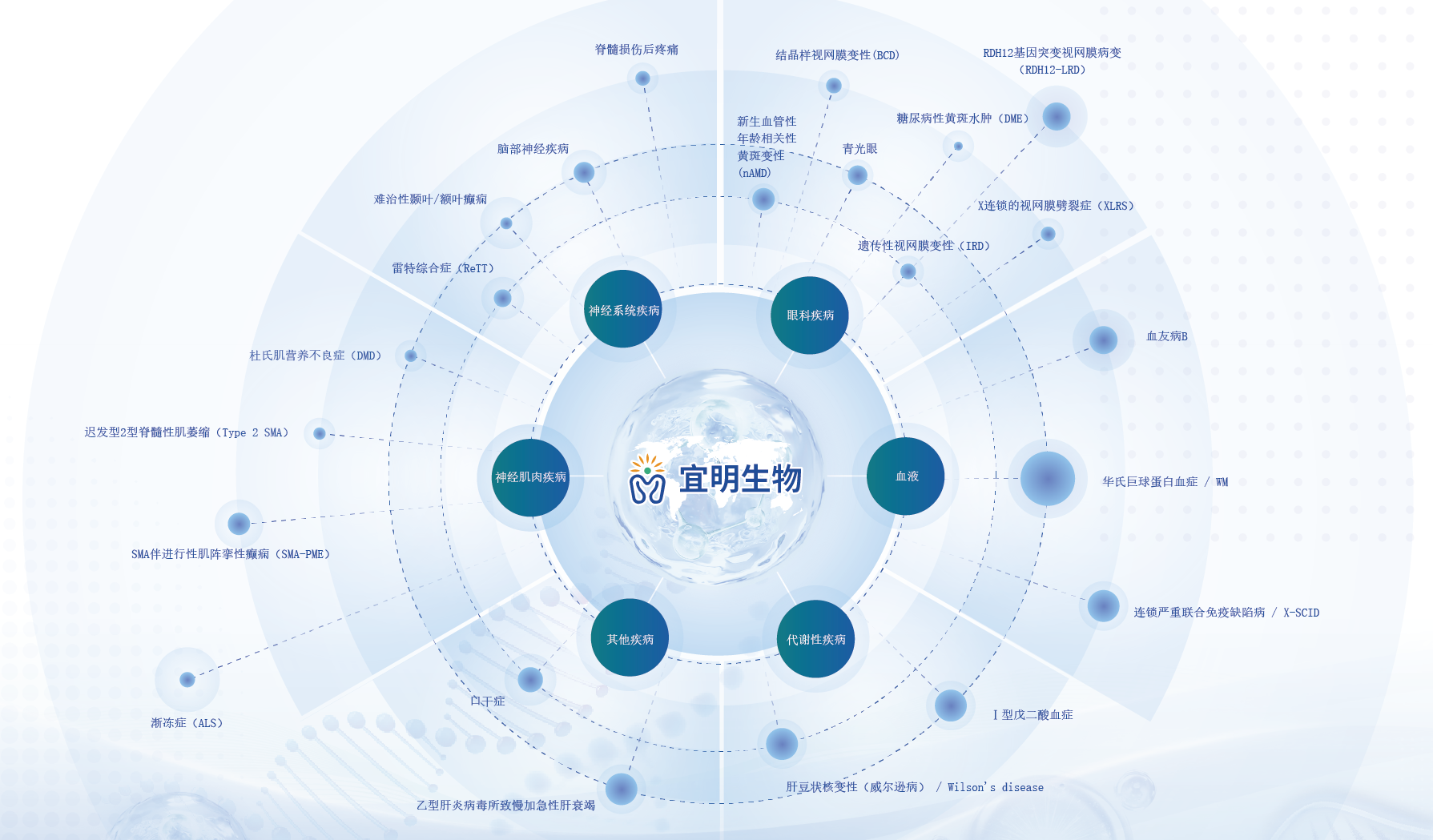
宜明生物病毒载体生产平台赋能数十种疾病治疗
全面布局下一代细胞治疗
自体CAR-T、通用型CAR-T、体内CAR-T是目前细胞治疗领域的三大重要技术路径:传统CAR-T聚焦个性化治疗;通用型CAR-T以“现货供应”为突破,实现规模化落地;体内CAR-T则以“体内直接改造”为核心,简化流程、降低成本。
然“不谋全局者,不足谋一域。” 宜明生物在筑牢传统CAR-T技术根基的同时,积极打造床旁CAR-T——作为传统自体CAR-T的安全、高效、低成本升级版。并依托自身病毒载体产业链优势,同步布局通用型CAR-T与体内CAR-T,形成 “传统CAR-T+床旁CAR-T+通用型CAR-T+体内CAR-T”全矩阵技术体系,全方位满足不同临床场景的需求。

宜明生物先进的自动化生产检测设备
一季度,宜明生物携手华夏英泰,共同开启“重度自免和肿瘤”的治愈征程。此次合作融合了华夏英泰的前沿管线与宜明生物病毒载体生产平台优势及全链条产业能力,精准直击自体细胞治疗的行业瓶颈,全力推动自免与肿瘤治疗领域的技术革新。
与此同时,宜明生物同步联动国际力量,与美国Cellinfinity BIO达成重磅合作,全力支持体内CAR-T前沿疗法的进一步开发与产业化落地。宜明生物的Ubri-LVVTurbo慢病毒生产平台,凭借显著的高效性、成本优势与全流程服务能力成为此次合作的关键赋能引擎。该平台整合悬浮培养、全封闭下游工艺及UltraCell™三大核心技术,产量较传统工艺提升5倍以上,成功将单剂CAR-T慢病毒载体成本降至100美元级别,约为行业平均成本的1/20。这一突破不仅重塑了细胞治疗的成本结构,更大幅提升了先进疗法的可及性。
进军再生医学新蓝海
诱导多能干细胞(iPSC)作为再生医学领域最具变革性的核心技术之一,在心衰、糖尿病、帕金森病等重大难治性疾病治疗中具备深远的临床价值与产业前景。布局iPSC 赛道,是宜明生物抢占下一代细胞治疗制高点、完善CGT 全产业链能力的关键战略落子。
历时两年的不懈技术攻关,宜明生物成功自主研发基于RNA-LNP的Ubri-iPSC®重编程技术,该技术采用非质粒非病毒载体系统,从根源规避传统质粒及病毒载体的基因组整合风险,并且突破性地实现了在外周血单核细胞(PBMC)中高效重编程,效率高达0.3%~0.5%,在成纤维细胞中,重编程效率更攀升到5%~10%,真正开启iPSC重编程领域的供体革命。这场革命的核心,是将PBMC确立为新一代起始细胞:相较传统成纤维细胞,PBMC来源更广、仅需微创取材,从根本突破临床取材限制,拓宽iPSC应用场景。目前该项技术完成了FDA DMF备案,具备国际化合规基础。
依托这项技术,公司还开发建立了成熟的干细胞(iPSC/ESC)定向分化技术平台(包括造血干/祖细胞、神经元、软骨细胞、少突胶质细胞,胰岛细胞等),持续推进再生医学领域布局。其中iPSC衍生的MSC及其外泌体等产品,可实现体外规模化、标准化扩增,具备“稳定可持续的细胞来源”与“多批次高度均一、质量稳定”的核心优势,有效解决传统成体干细胞来源有限、批次差异大等行业关键痛点。
同时,为了支持临床前的科学探索,公司同步推出Ubri-Amrita™ iPSC重编程RNA-LNP试剂盒,实现从科研到产业全链条护航,为干细胞治疗标准化生产提供关键支撑,让自体iPSC细胞药物成为现实。

一季度,宜明生物与多家战略合作伙伴达成重要合作,正式进入iPSC治疗与再生医学领域。宜明生物从细胞重编程、细胞建库、定向分化至制剂生产的全链条CDMO服务,高效打通前沿科研到临床转化的完整路径,助力下一代细胞治疗迈向全新未来。
从中国走向世界,拓展全球化服务生态
本季度的合作版图不仅深耕国内市场,更广泛联动全球创新力量,涵盖来自加拿大、美国、芬兰、德国等多家海外创新药企。既助力本土创新成果稳步出海,也积极引入国际前沿技术与理念落地中国,为ATMP行业持续搭建创新共赢的坚实桥梁。在CGT全球化浪潮中,宜明生物,正成为链接“创新与市场”、贯通“中国与世界”的桥梁。
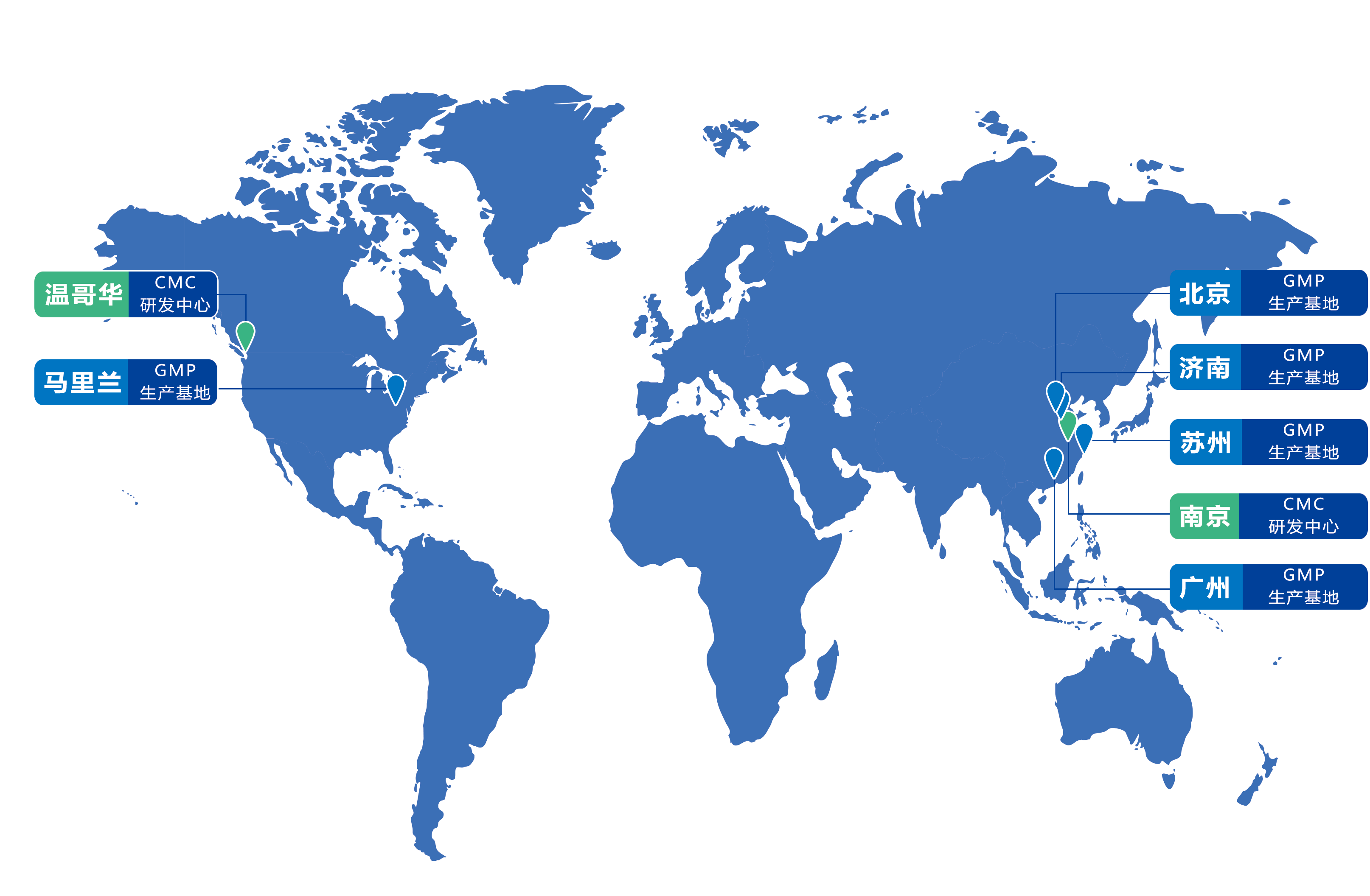
全球化产能网络,确保了“中美协同,多地联动”。宜明生物在北京、苏州、济南、广州及美国马里兰布局五大GMP生产基地。其中,苏州、济南及美国马里兰基地均已完成FDA DMF备案,苏州基地更顺利率先通过EU GMP QP认证,具备完善的国际化申报与供应资质,为全球化布局奠定了坚实的合规根基。
尤为重要的是,马里兰基地作为中国药企“出海”的本地化生产“桥头堡”,精准破解了国内药企“出海”过程中面临的异地监管、本地化生产、供应链重构及工艺落地等核心痛点,将原本复杂繁琐的“从0起步”,转化为“即插即用”的便捷化服务。国内药企无需在美建厂,可藉马里兰基地作为海外生产与运营支点,顺利完成工艺转移与工艺锁定,实现美国本土化生产,有效降低出海门槛与周期,并为后续大规模全球化发展奠定基础。

宜明生物马里兰GMP生产基地
全面助力跨境产业化,让中国创新走向世界。宜明生物可为国内药企提供从工艺转移、海外放大生产到FDA申报的全流程支持。依托美国基地的本地化产能与合规经验,实现“国内早期开发+美国规模化生产”协同模式,显著降低国际化成本与周期,加速创新药全球落地,显著降低国际化落地的门槛与时间成本。
全领域、全链条技术平台,国际化合规体系,厚积薄发。宜明生物构建了质粒载体、病毒载体、细胞药物及核酸药物四大GMP生产平台,形成覆盖临床前研究、临床试验至商业化生产的全周期服务体系。“博观而约取,厚积而薄发”,多年来在工艺开发与质量控制上的持续投入,如今已转化为服务全球客户的坚实底气。
为助力创新药企高效开展全球临床试验、加速注册申报,宜明生物已经完成近20项FDA DMF备案,覆盖关键原材料、生产基地与质量控制体系,相关备案号已在多个IND项目申报中成功引用。宜明生物中美申报团队拥有丰富的中美欧多国申报实战经验,精准把握各个监管机构的体系要求,目前已助力国内外多家药企获得数十项IND批件,推动多个项目进入临床试验阶段。
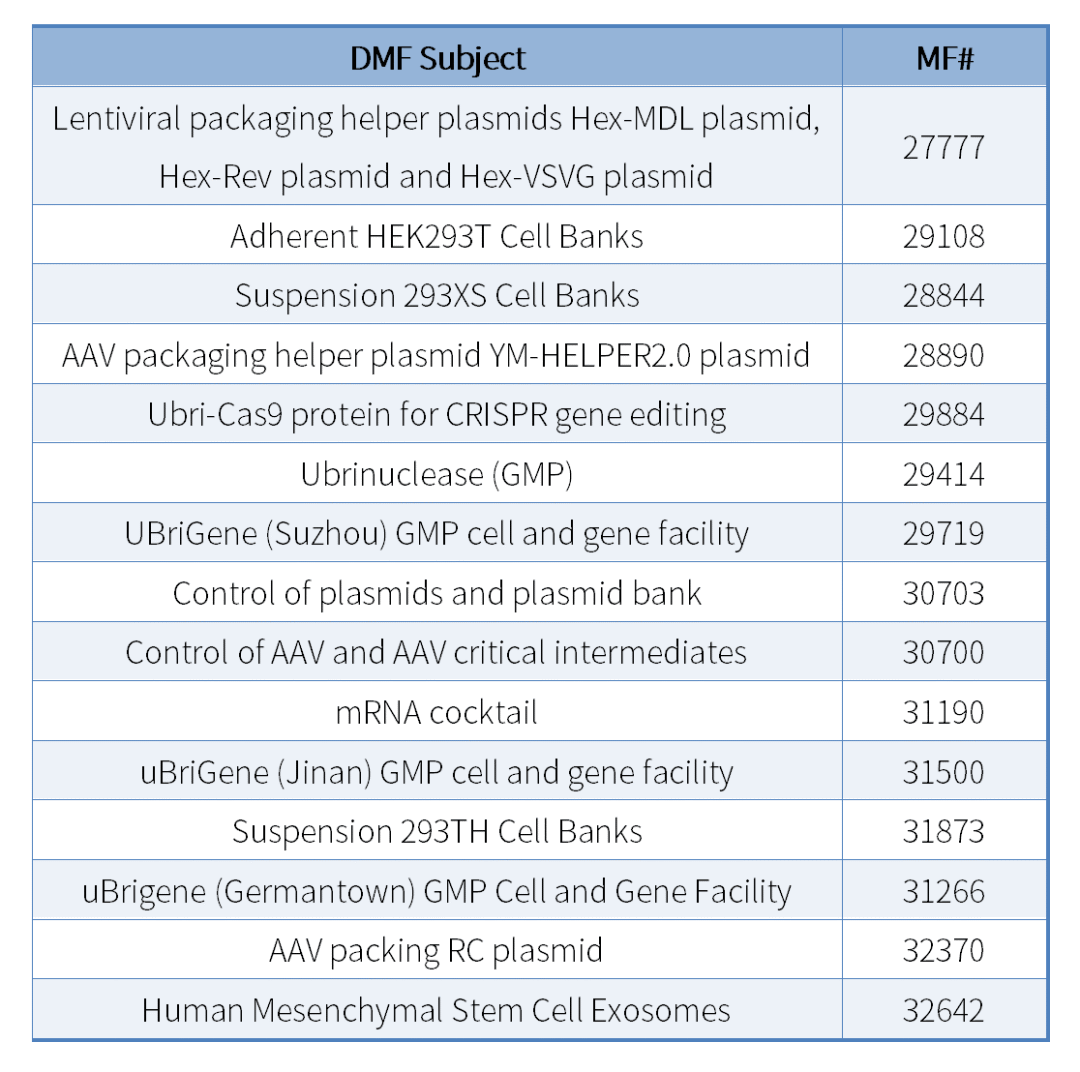
宜明生物DMF备案库(部分展示)
结 语
战首季、启新局、建新功。2026 年第一季度,宜明生物全线高燃开局:前沿赛道捷报频传、重磅合作接连落地,产业版图与全球化服务能力同步跃升。
“雄关漫道真如铁,而今迈步从头越。”站在新的起点,宜明生物依托中美双基地布局、多国合规体系与全链条技术平台,助力客户实现“国内研发制备、美国规模化生产”,中美协同申报,打通创新药全球化高效通路。
未来,宜明生物将继续坚守“双向赋能、合作共赢”理念,在“出海”与“入海”的双向航道上稳步前行,以更强产能、更严合规、更前沿技术,与全球伙伴携手推动先进疗法惠及患者,共筑CGT产业高质量发展的全球化新未来。
让生命更健康,让世界更美好!
关于宜明生物
宜明(北京)生物医药股份有限公司(简称“宜明生物”)成立于2015 年,是一家致力于先进治疗药品(ATMP) 的技术开发和应用,提供一站式CRDMO整体解决方案的全球化企业。宜明生物在美国马里兰,中国北京、苏州、济南和广州建立GMP生产基地,总面积超30,000平米,配备50+条生产线,涵盖质粒、病毒载体、细胞治疗药物及RNA药物临床及商业化生产,并在温哥华、南京设立了专注于前瞻性技术开发应用的全球研发中心。已承接/交付临床级产品(IIT/IND/I-II期)百余批次,帮助客户完成数十项创新药物IND获批临床。宜明生物依托国际化的专家团队及全球化布局的研发与生产基地,打造符合国际标准的CRDMO平台,为全球ATMP企业提供从早期研发、工艺开发、临床研究(IIT/IND/I-III期)到商业化生产的一站式解决方案。

service@ubrigene.com
热线:400-077-2366

