CDMO服务
GMP级生产制备平台,先进治疗药品走向世界和商业化的桥梁
环状RNA(circRNA)分子是一类不具有5'末端帽子和3'末端poly(A)尾巴、并以共价键形成封闭环形结构的RNA分子。与mRNA相比,环状RNA具有在生物体内高稳定性、低免疫原性等优势,可广泛应用在癌症、再生医学、蛋白质替代、传染病和自身免疫疾病等多个领域。
与线性RNA相比,环状RNA是一种闭环结构,不需要帽子结构或polyA尾。由于没有游离末端,环状RNA能够抵抗RNA外切酶的作用,在细胞内更加稳定。
| mRNA | 环化RNA | |
| 功能 | ||
| 标准真核mRNA结构可进行短时间蛋白表达 | 可编码表达蛋白 不编码起调节作用 | |
| 表达机制 | ||
| 5’帽子结构+Kozak翻译起始位点 | IRES | |
| 诱导/靶向能力 | ||
| 无 | 有可能,依赖于不同的IRES序列 | |
| 所需工具酶 | ||
| 加帽酶或帽子类似物 | 核酶,去除线性RNA的酶(如RNaseR) | |
| 所需其他序列 | ||
| 5’-UTR,3’-UTR,PolyA尾 | 核酶序列 | |
| 胞内稳定性 | ||
| 低(一周内),依赖加帽效率和长polyA | 高(两周左右),无需帽子和polyA结构 | |
| 编码序列限制 | ||
| 长,取决于体外转录酶的上限 | 随长度增加成环效率下降 | |
| 产量 | ||
| 体外转录产量高 | 体外转录产量高,但成环底物浓度受限,成环效率低 | |
| 成本 | ||
| 中等 | 取决于制备方法 | |
| 表达强度 | ||
| 瞬时表达强度高,下降速度快 | 瞬时表达强度相对弱一些,但持续性好 | |
| 免疫活性 | ||
| 高 | 低 | |
| 应用场景 | ||
| 需快速表达大量蛋白的应用 | 需在细胞内稳定存在时间更长的应用 |
宜明生物可提供多种制备circRNA的策略方案,分别基于PIE(内含子-外显子剪接)的环化策略和基于细胞内自环化的的策略:
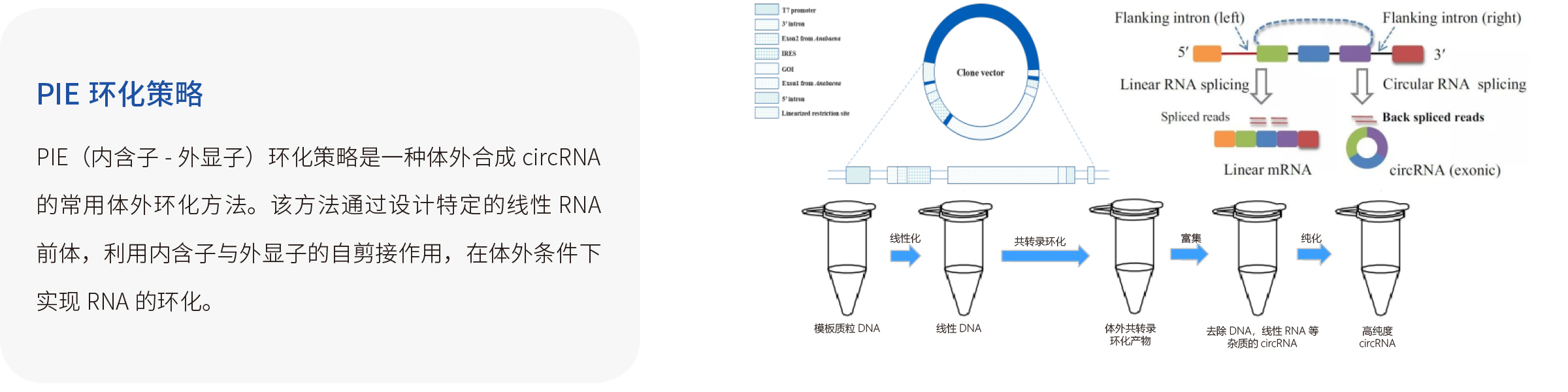
PIE环化策略:PIE(内含子-外显子)环化策略是一种体外合成circRNA的常用体外环化方法。该方法通过设计特定的线性RNA前体,利用内含子与外显子的自剪接作用,在体外条件下实现RNA的环化。
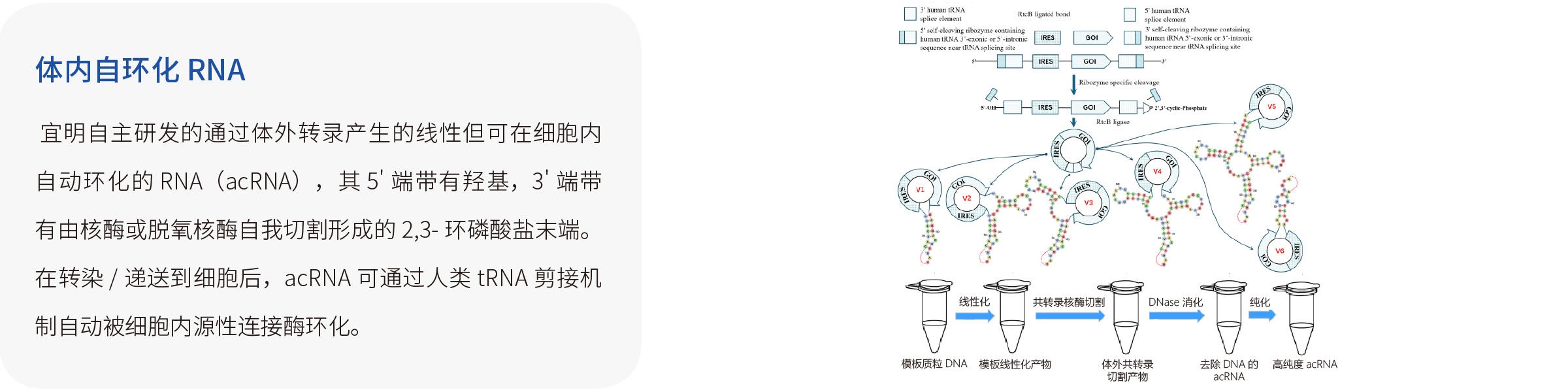
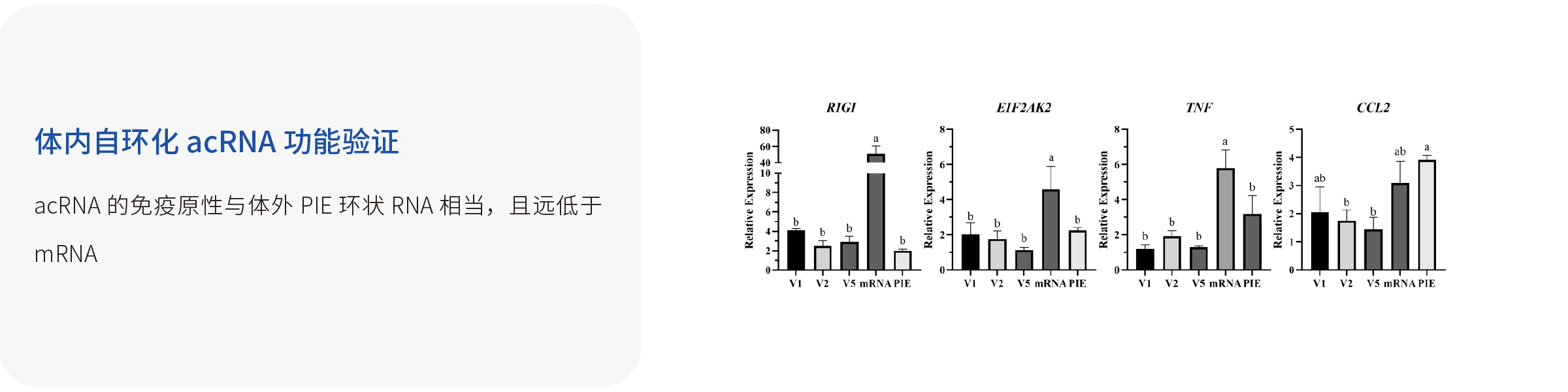
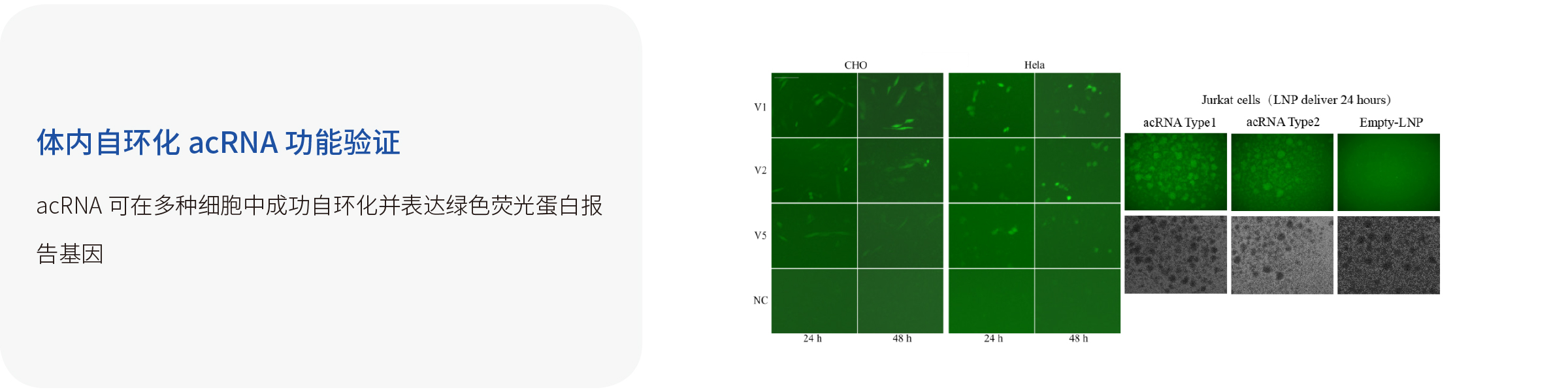
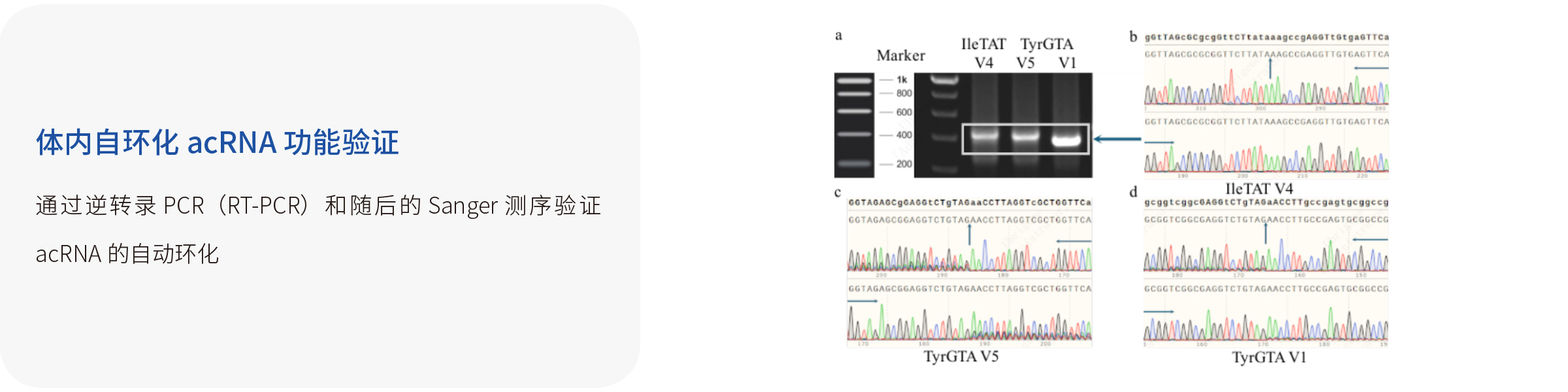
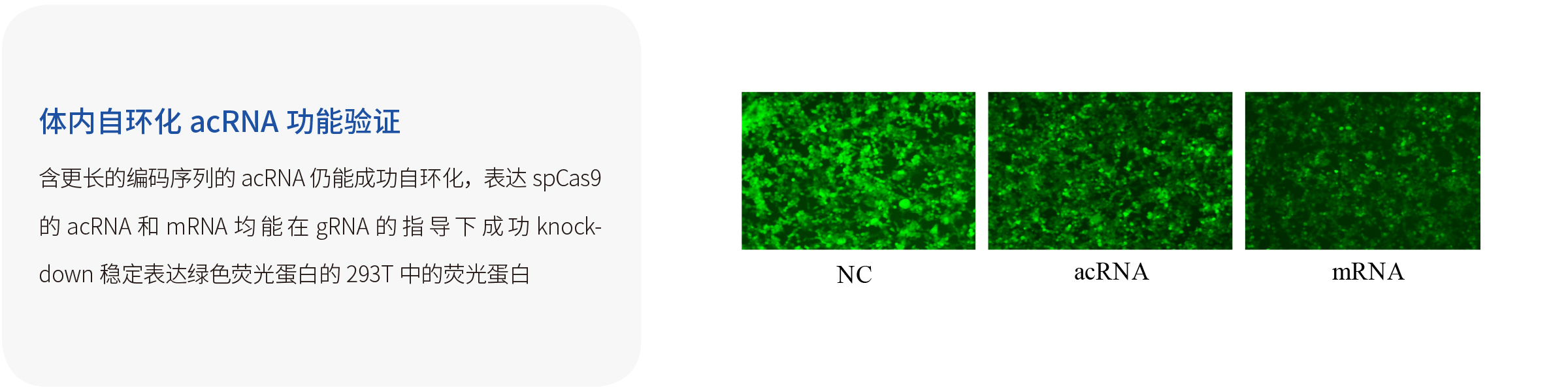
体内自环化RNA:宜明自主研发的通过体外转录产生的线性但可在细胞内自动环化的RNA(acRNA),其5'端带有羟基,3'端带有由核酶或脱氧核酶自我切割形成的2,3-环磷酸盐末端。在转染/递送到细胞后,acRNA可通过人类tRNA剪接机制自动被细胞内源性连接酶环化。
以上两种环化RNA均在内部核糖体进入位点(IRES)元件的驱动下表达编码的蛋白质。
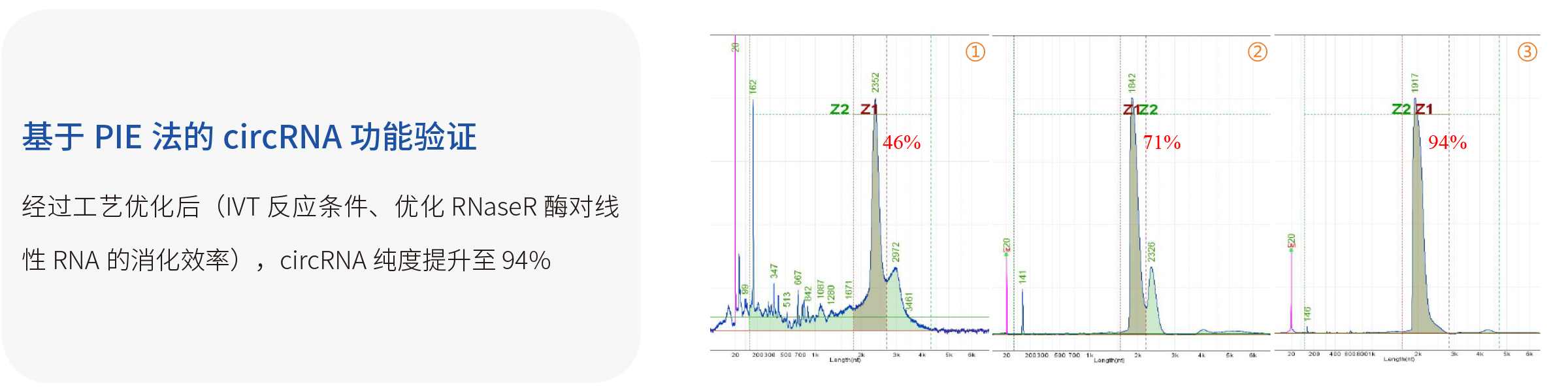
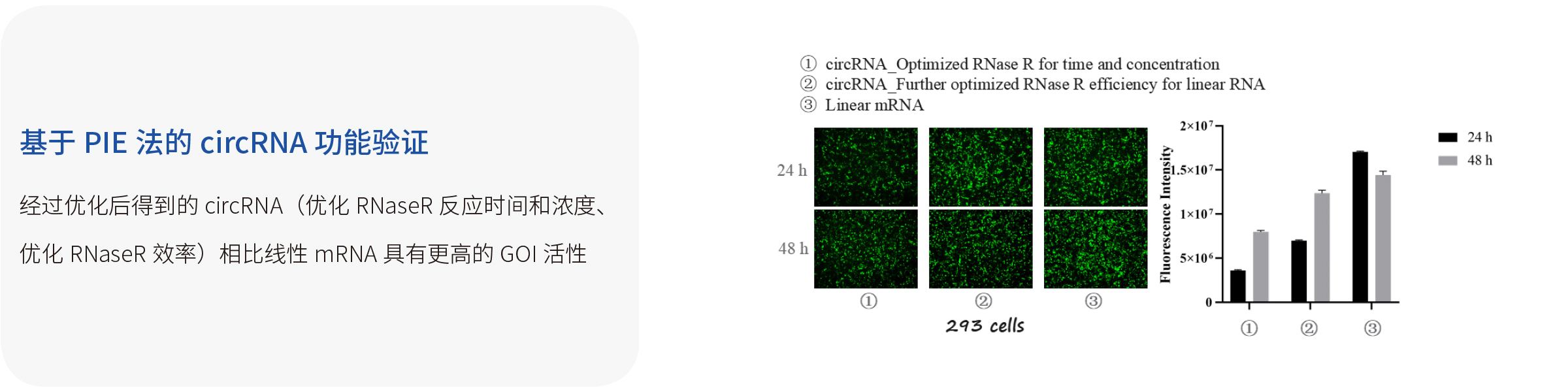
| PIE体外环化RNA | 宜明生物的acRNA | |
| 简介 | ||
| 体外转录中和转录后内含子核酶剪接成环 | 进入细胞后通过内源性连接酶催化完成环化 | |
| 表达机制 | ||
| IRES | IRES | |
| 诱导/靶向能力 | ||
| 有可能,依赖于IRES序列 | 有可能,依赖于IRES序列和自环化接头元件 | |
| 所需工具酶 | ||
| RNaseR | 无需RNaseR | |
| 胞内稳定性 | ||
| 高,无需帽子和polyA结构 | 细胞内成环后高,无需增加额外加帽和加尾工艺 | |
| 编码序列限制 | ||
| 随长度增加成环效率大幅下降,通常在10K以内 | 随长度增加成环效率下降,通常在10K以内 | |
| 产量 | ||
| 体外转录产量高,但成环底物浓度受限,成环效率低,副产物不易去除 | 体外转录产量高,自环化最终效率取决于细胞类型,有较多的可筛选性和针对性优化的可能性。 | |
| 成本 | ||
| 高 | 低 | |
| 表达强度 | ||
| 瞬时表达较强,有可能达到类似mRNA水平,持续性好 | 瞬时表达较mRNA弱,持续性好 | |
| 免疫原性 | ||
| 低,但可能残留人工接头序列 | 低,接头为人源化序列,理论上更安全 |