近日,宜明生物成功完成人间充质干细胞外泌体(Human Mesenchymal Stem Cell Exosomes)的美国FDA DMF(Drug Master File,药品主文件)备案,备案号为DMF32642。
本次DMF备案成功,表明宜明生物的外泌体生产工艺、质量控制已获得国际认可。未来,合作客户可直接引用该DMF备案号,将大幅简化IND申报资料包,缩短审评周期,为创新药品的全球开发按下"加速键"。

间充质干细胞外泌体是从间充质干细胞培养上清液中分离纯化的细胞外囊泡,直径30-150nm,属于细胞外囊泡(EVs)的核心类型。外泌体凭借其微小的体积,携带脂类、蛋白质、核酸 (DNA和RNA)等多种“精准信使”分子,可自由穿梭在细胞间,充当“信息传递员”,参与细胞增殖与凋亡、转移与侵袭、免疫应答、细胞分化、代谢调控等生理过程。
宜明生物依托国际化的研发团队与完善的产业化平台,已构建起覆盖外泌体研发、生产、质控的全链路体系。随着科研与产业的深度融合,外泌体作为新一代生物活性载体,有望在再生医学与生物科技领域扮演更重要的角色。
伴随先进治疗产品(ATMP)的全球化,DMF备案已成为中国药企"出海"的关键战略资产。截至目前,宜明生物已累计完成近20项核心技术模块与生产设施的FDA DMF备案,构建起覆盖ATMP全生命周期的服务网络。
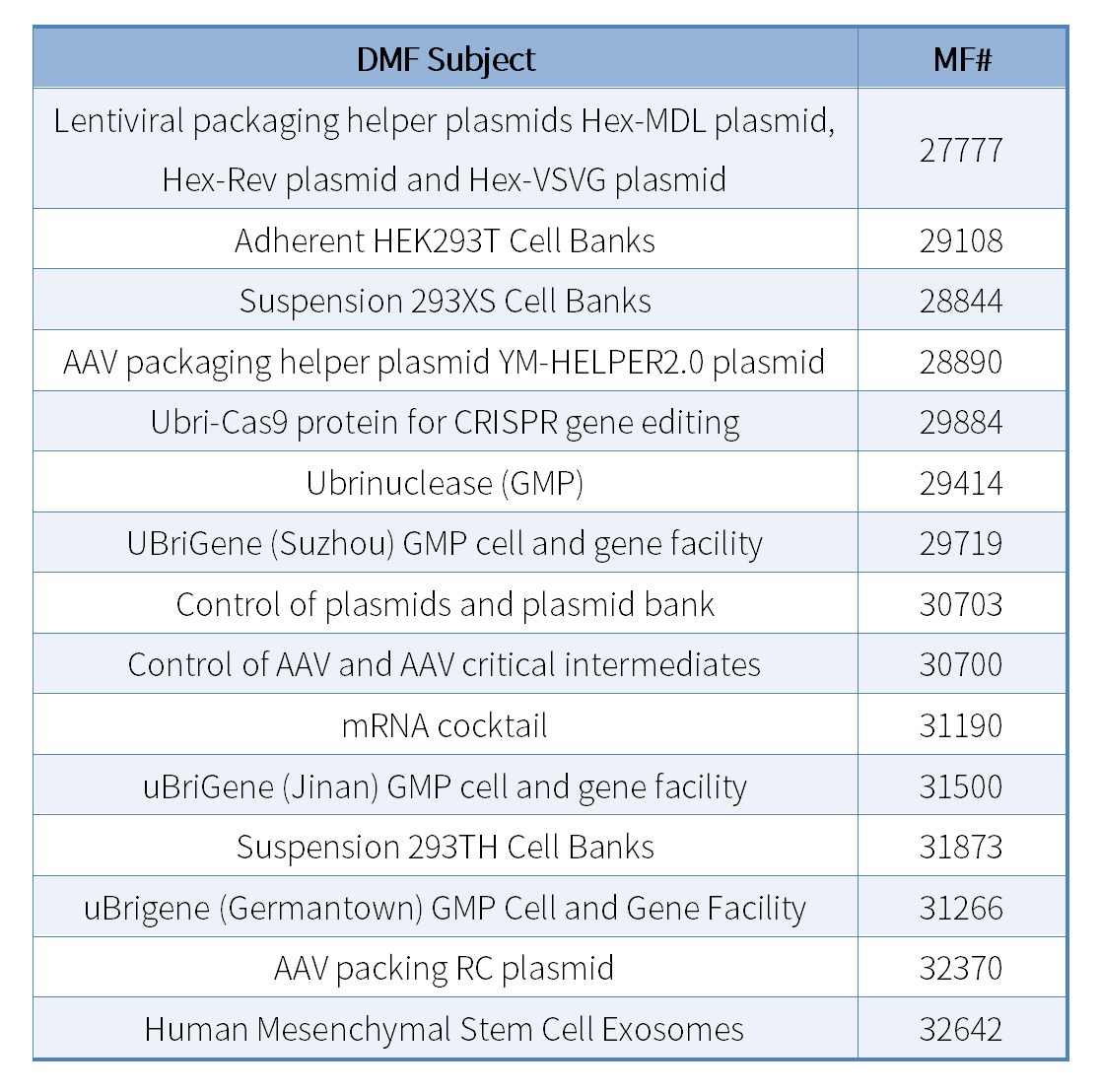
图示:宜明生物DMF备案库(部分展示)
这一系列备案不仅是平台技术实力的集中体现,更意味着宜明生物通过标准化、模块化的技术组件,为客户提供经FDA前置审阅的核心生产要素,系统性降低细胞与基因治疗药物的开发门槛与时间成本,助力更多创新疗法快速迈入临床、走向全球。

关于宜明生物

宜明(北京)生物医药有限公司(简称“宜明生物”)成立于2015 年,是一家致力于先进治疗药品(ATMP) 的技术开发和应用,提供一站式CRDMO整体解决方案的全球化企业。宜明生物在美国马里兰,中国北京、苏州、济南和广州建立GMP 生产基地,总面积超30,000平米,配备50+条生产线,涵盖质粒、病毒载体、细胞治疗药物及 RNA 药物临床及商业化生产,并在温哥华、南京设立了专注于前瞻性技术开发应用的全球研发中心。已承接/交付临床级产品(IIT/IND/I-II期)百余批次,帮助客户完成数十项创新药物IND获批临床。宜明生物依托国际化的专家团队及全球化布局的研发与生产基地,打造符合国际标准的CRDMO平台,为全球ATMP企业提供从早期研发、工艺开发、临床研究(IIT/IND/I-III期)到商业化生产的一站式解决方案。

service@ubrigene.com
热线:400-077-2366

